细胞的物质基础
1. 组成细胞的元素/化学键
离子键,盐键(生物only),共价键,氢键,范德华力
2. 糖类: 多羟醛/酮+其聚合/衍生物
2.2. 单糖的化学结构
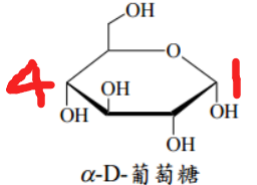
1️⃣链状结构
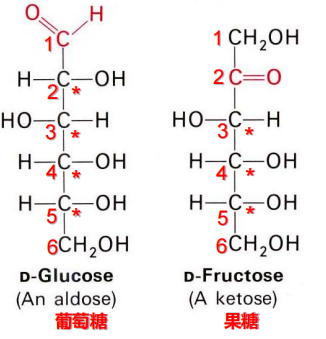
2️⃣
分型(注意定义)
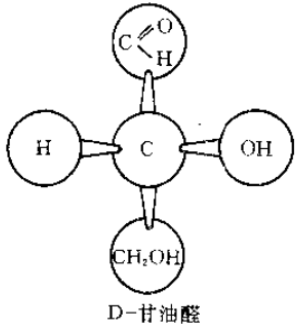
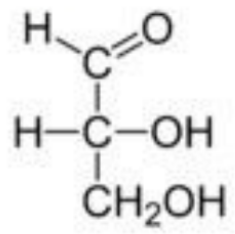
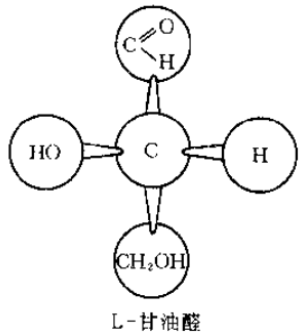
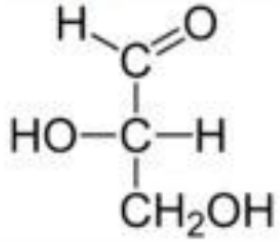
甘油醛的
分型
手性碳( )相连的 构型 结构图(甘油醛) 分子式 右 左 单糖的
分型 ( 型糖最常见)
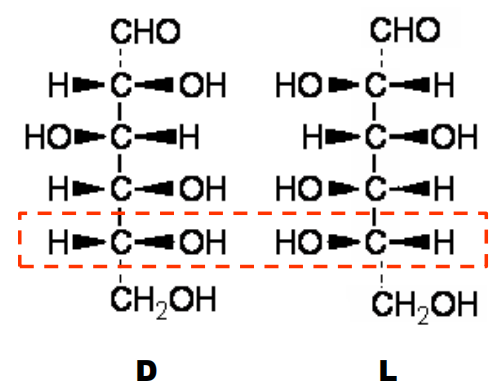
分型规则: 离羟基最远的不对称碳原子上羟基的空间排布与甘油醛比较,确定类型
单糖溶液变旋性:
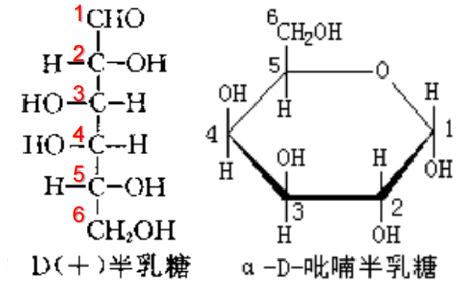
3️⃣环状结构
成环示意图
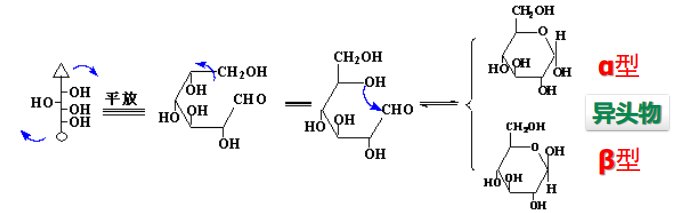
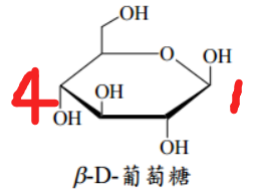
环状结构分类,注意
类型:
构型 新生成的羟基( 号碳) 对面羟基( 号碳)位置 相同 不同 4️⃣环状糖分子的
式(基准-规则-示例)
基准
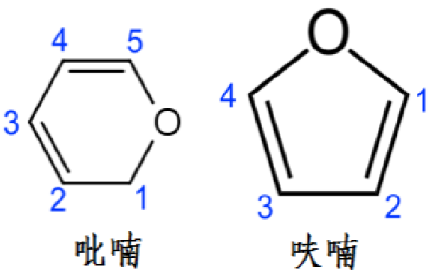
书写规则
顺时针书写
式左侧基团 (羟基)书于环平面之上,右侧基团书于环平面之下
型糖环外基团书于环仠面之上, 型在平面之下
示例
2.3. 单糖的化学性质
反应类型 描述 结果 成酯 含有醇羟基的化合物与酸反应生成酯 生成酯类化合物 成苷 醇羟基与糖反应生成苷 生成苷类化合物 脱氧 某碳上的羟基被氢原子取代 生成脱氧糖(如 脱氧核糖) 氨基化 羟基被氨基取代 生成含有氨基的化合物 差向异构 葡萄糖在碱性条件下 转变为 甘露糖和 果糖 葡萄糖转化为 甘露糖和 果糖 2.4. 麦芽糖的性质
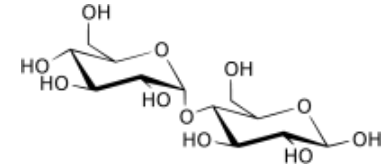
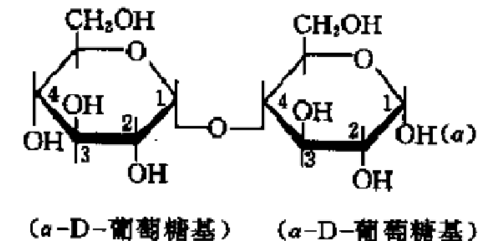
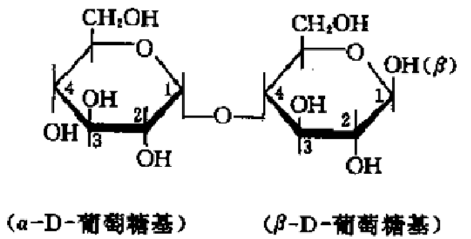
2.4.1. 结构
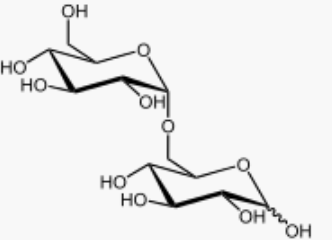
类型 两个葡萄糖连接 结构 正常麦芽糖 糖苷键 异麦芽糖 糖苷键 2.4.2. 种类
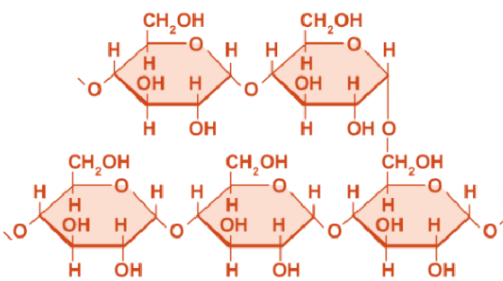
麦芽糖 麦芽糖 2.5. 多糖结构与性质
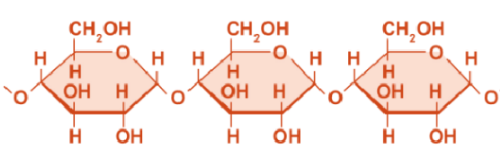
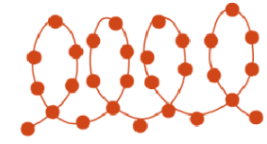
1️⃣淀粉:直链
支链( 糖苷键)
结构 架构 直链淀粉 支链淀粉 2️⃣糖原:
3️⃣纤维素:
3. 脂肪类
3.0. 概述
1️⃣功能:构成生物膜,保护内脏,储能,传递信号(固醇类激素),电热绝缘
2️⃣定义:
以上脂肪酸 醇类:如甘油醇、鞘氨醇
醇类组成的酯类及衍生物/类似物
3.1. 脂结构与分类
1️⃣脂肪酸
分为饱和/不饱和(有双键),
数 最常见,熔点饱和 不饱和(顺式 反式),必需脂肪酸如海洋 尤其注意,不饱和的/名字中带亚的,大概率是必需脂肪酸
2️⃣单脂(
一/二/三酰 甘油): 高级醇 个脂肪酸
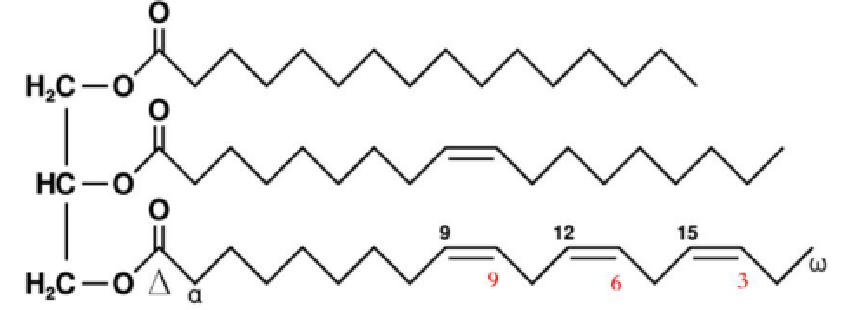
3️⃣复脂类(磷脂/糖脂):含有磷酸/糖类的脂类,甘油
磷脂/糖脂 4️⃣固醇类:高级一元醇,可转化为类固醇激素/维生素/合成胆汁酸
3.2. 脂理化性质
1️⃣物理性质: 无色无味,中性,密度小于水,不溶于水
2️⃣化学性质:
可氧化

可与碱皂化:皂化价衡量㒵化
油脂所需多少 的
4. 蛋白质
4.0. 概述
1️⃣定义:氨基酸通过肽键连接而成的生物大分子
2️⃣作用: 结构物质,功能载体,生命起源
3️⃣组成:
4.1. 氨基酸
1️⃣生物体内的
种氨基酸(都是 型) 2️⃣氨基酸分类
非极性脂肪族
极性中性氨基酸:侧链基团含有 极性,只含 非极性 芳香族侧链氨基酸: 侧链基团含有苯环
酸碱性氨基酸: 酸性(侧链含
),碱性(侧链含 ) 3️⃣人体必需氨基酸
甲硫氨酸、缬氨酸、赖氨酸、异亮氨酸、苯丙氨酸、亮氨酸、色氨酸、苏氨酸
4️⃣氨基酸的等电点(必考)
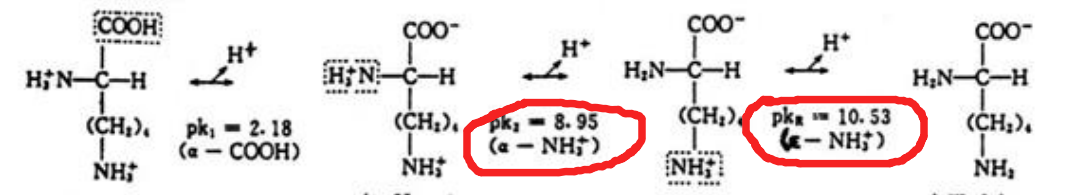
定义: 氨基酸中
和 数目相等时溶液的 氨基酸等电点 公式:
净电荷为 净电荷为 性质: 例如将氨基酸溶于水
说明解离出 多带负电 要让其等电还得加 则其等电点小于 PS特殊情况:如有多步只取电中性分子两端的
5️⃣ 氨基酸的化学性质:氨基-形成西佛碱,氨基-苯异硫氰酸,羧基-成脂,成肽键
4.2. 多肽
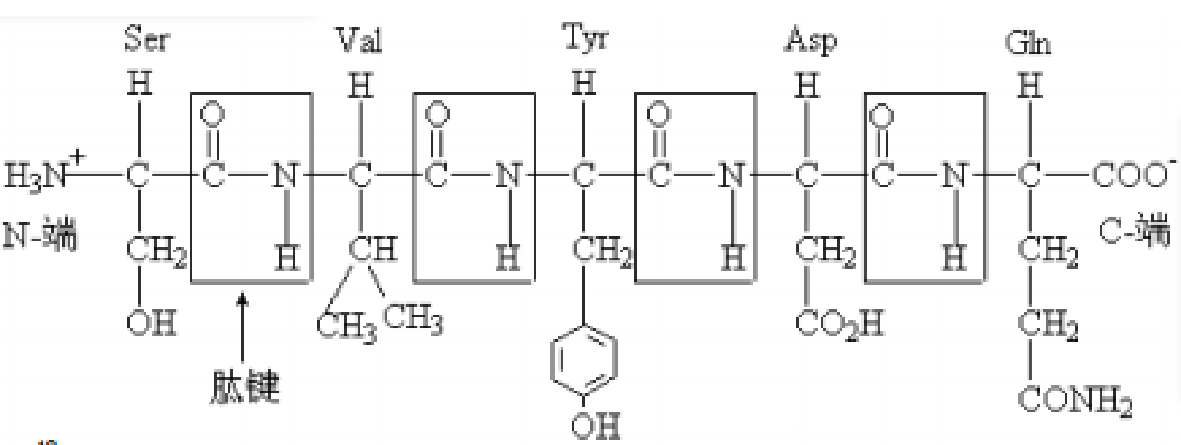
1️⃣书写规则: 左
右, 端 端 2️⃣结构特性:
肽键中
性质类似于 不能自由旋转,六个原子共平面(肽平面)
4.3. 蛋白质
4.3.1. 蛋白质结构
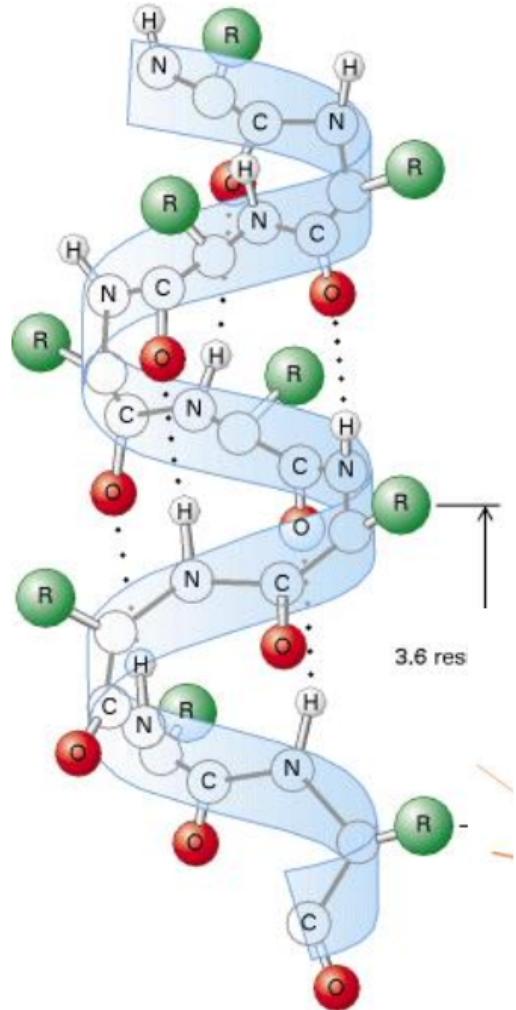
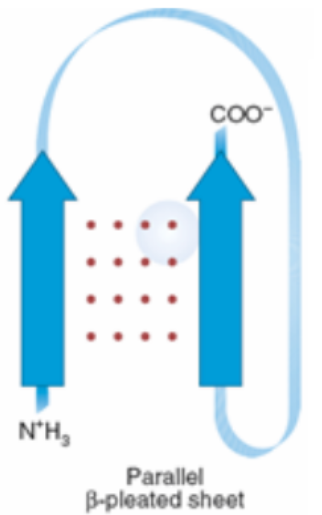
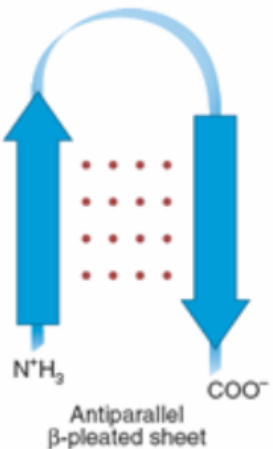
结构级别 描述 一级结构 肽链 二级结构 螺旋, 转角, 折叠 三级结构 三维结构,蛋白质的单个多肽链水平 四级结构 由多个三级结构拼接组成 1️⃣二级结构中
特点
(右手)螺旋 折叠(反平行) 折叠(平行) 2️⃣超二级结构(模体
):蛋白分子中几个二级结构片段缠绕产生功能 3️⃣蛋白质三级结构的化学键或作用力:静电(盐键),共价,氢键,疏水键
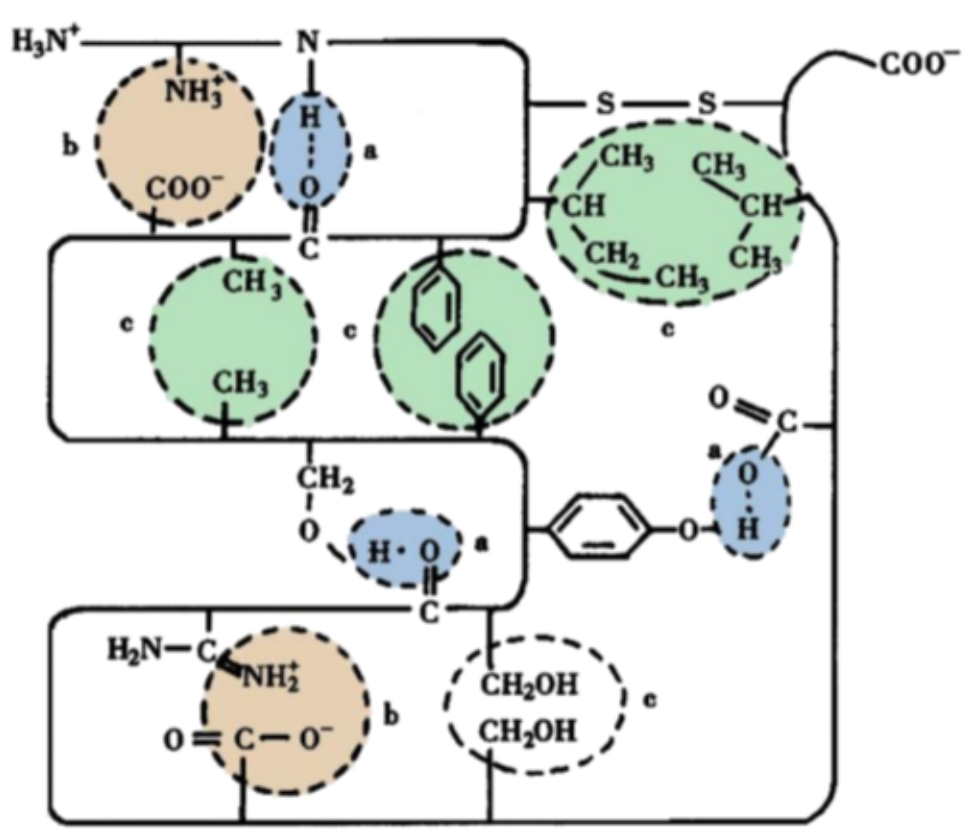
4️⃣蛋白质四级结构中的一些效应
别构效应:蛋白质
分子功能改变 血红蛋白
效应:
注意
增多都会导致平衡右 释放 血红蛋白的
作用机制: 结合血红蛋白 降低对氧亲和力 释放更多氧到周围组织 4.3.2. 蛋白质结构与功能
1️⃣结构决定功能,但不完全决定
2️⃣一级结构决定高级结构,一级结构相同二级结构不同影响生理功能,高级结构(别构效应等)
4.3.3. 蛋白质的物理性质
特性 描述 紫外吸光 在 处吸光,主要由氨基酸中的苯环贡献 变性 通过射线、酸碱等外部因素引起的结构变化,不影响一级结构 4.3.4. 全酶(结合酶)
蛋白质(酶蛋白)
热稳定小分子(辅因子)
5. 核酸:自然界先有核酸再有蛋白质
5.1. 核酸组成结构
5.1.1. 核糖
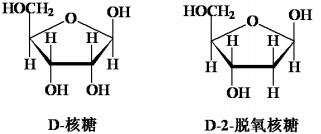
5.1.2. 碱基
1️⃣嘧啶:尿里两泡泡(
),胸前一滩尿( 是 的前体),尿上是个氨气包( )
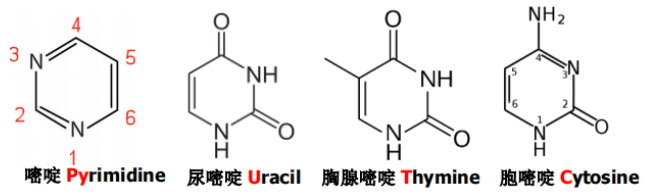
2️⃣嘌呤:鸟儿张嘴吸氨气(
),线下来把鸟儿替( )
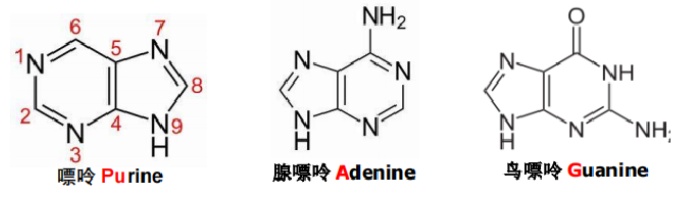
5.2. 核酸一级结构

1️⃣连接方式:
与 磷酸酯键相连 2️⃣书写规则: 如
5.3. 核酸高级结构(DNA双螺旋结构)

1️⃣一般结构:
碱基位于内侧,磷酸脱氧核糖在外
碱基环平面与螺旋轴垂直,糖基环平面与碱基环平面成
角 2️⃣特殊结构:三螺旋,四股螺旋
5.4. DNA的理化性质
插入一下:
易水解,不稳定,不适合做遗传物质 5.4.1. 含氮碱基的紫外吸收
样品类型 蛋白质样品
吸收峰是
(区别于蛋白质 )
代表吸收光强, / 代表波长,这种特性用于提纯 5.4.2. DNA变性与复性:指的是双链的打开与还原
1️⃣
的变性在很窄温度区间内完成,称之为DNA熔点 2️⃣
含量越高, 越难变性 5.4.3. PCR
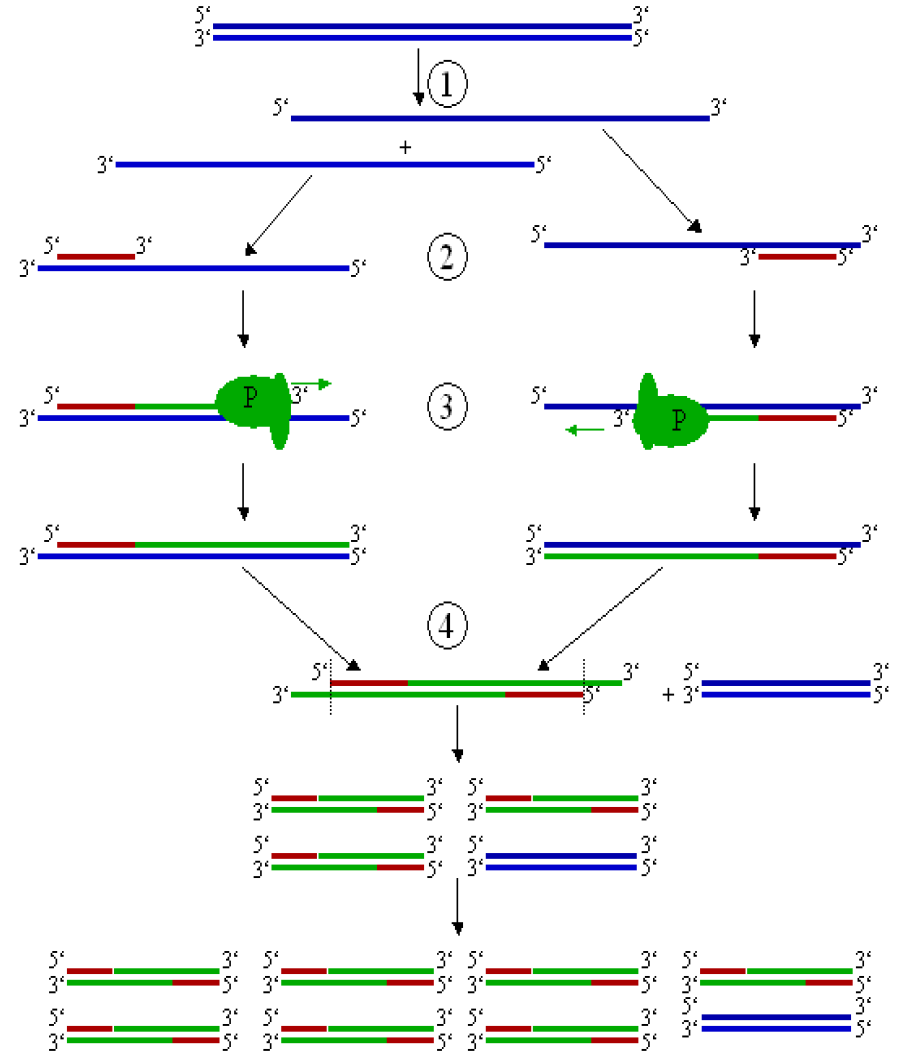
1️⃣
变性 双股 打开 2️⃣约
退火 引物与模板 配对结合 3️⃣在
时 延长 聚合酶
温度 操作 操作的细节 变性 双股 打开 约 退火 引物与模板 配对结合 延长 使用 聚合酶 进行链延长 第一循环完成,两段双股
又可当作下一个循环模板,每次循环都使得扩增的 片段加倍